2020年09月29日 Eton Pharmaceuticals公司宣布,美国食品和药物管理局(FDA)已批准Alkindi Sprinkle(hydrocortisone)氢化可的松口服颗粒剂,作为一种替代疗法,用于治疗17岁以下肾上腺皮质功能不全(Adrenocortical Insufficiency,AI)儿童。
- Alkindi Sprinkle是第一个也是唯一1个获FDA批准的氢化可的松颗粒剂,专门用于治疗AI儿童患者。
Alkindi Sprinkle口服颗粒剂的批准,得到了6项临床研究的支持,其中包括第一个也是唯一1个评估口服氢化可的松治疗新生儿至8岁以下儿童AI的介入性III期研究。
在Alkindi Sprinkle获得批准之前,口服氢化可的松是仅5mg及更高剂量的片剂制剂获得了FDA批准。许多儿科患者需要低剂量和精确滴定的灵活性。因此,照料者必须切割或分割高规格氢化可的松片剂,以达到幼儿所需的低剂量,这可能导致剂量不准确。
Alkindi Sprinkle(hydrocortisone)口服氢化可的松颗粒剂 是一种速释口服氢化可的松颗粒制剂,在室温下的保质期为3年,不需要冷藏。
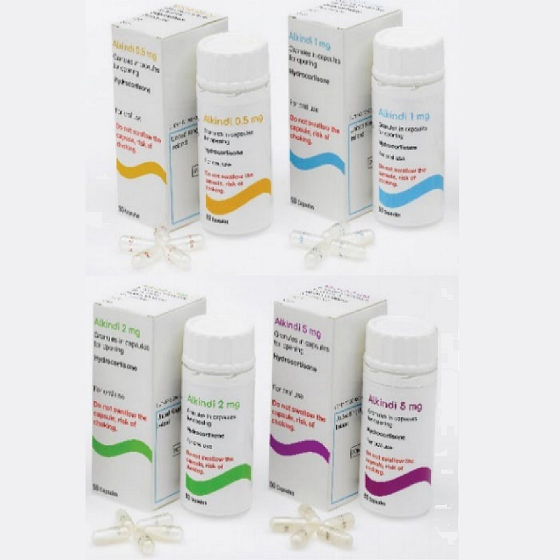
Alkindi Sprinkle采用经商业验证的技术制造,有4种强度:0.5mg、1mg、2mg、5mg,将使临床医生能够根据每例患者的需要,根据剂量和给药说明进行个体化给药。Alkindi Sprinkle预计将在2020年第四季度上市。
小儿肾上腺皮质功能不全(AI)是一种罕见的疾病,其特点是无法合成和释放氢化可的松(皮质醇),有时甚至是醛固酮。这会导致雄性激素过多(女性性发育异常、青春期提前、生长终止和身材矮小)。儿童AI最常见的形式是先天性肾上腺增生(CAH),它是由基因缺陷引起的。原发性或中枢性(二级和三级)AI患者体内皮质醇水平不足。体内皮质醇的减少可能会导致致命的后果,如肾上腺危象。为了生存,AI患者必须每天补充皮质醇。
 扫一扫
扫一扫 


