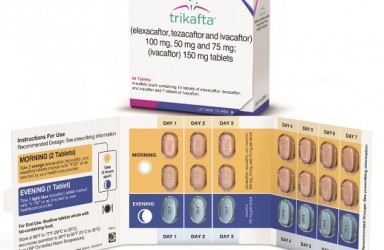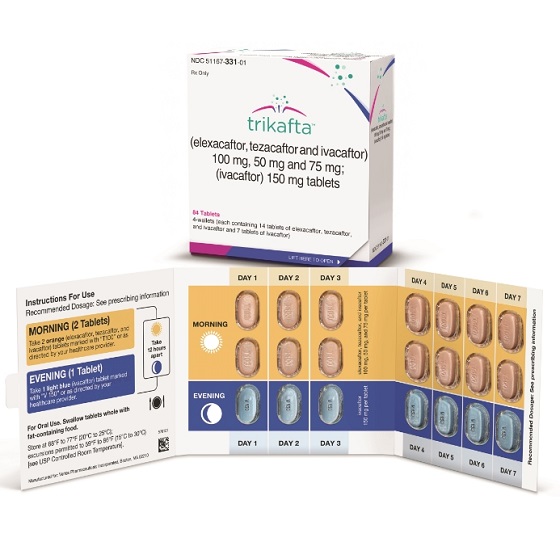
2019年10月21日,美国食品和药物管理局(FDA)批准Vertex制药公司的Trikafta(elexacaftor/tezacaftor/ivacaftor)用于治疗囊性纤维化(CF)跨膜传导调节因子(CFTR)基因中存在至少一个F508del突变、年龄≥12岁的CF患者.
- F508del突变是导致囊性纤维化(CF)的最常见突变。Trikafta用于携带一个F508del突变和一个最小功能突变的患者,或携带2个F508del突变的患者。
此前FDA已授予Trikafta优先审查资格、快速通道资格、突破性药物资格(BTD)。Vertex公司在提交Trikafta新药申请(NDA)3个月后便收到了FDA的批准,该批准较FDA审批计划目标日期大大提前了5个月,创下了FDA审批速度的新纪录。
在美国,Trikafta 预计定价为31.1万美元。
囊性纤维化(CF)是由囊性纤维化跨膜电导调节因子(CFTR)基因突变导致CFTR蛋白功能缺陷或缺失所致的罕见遗传性疾病。CFTR蛋白通常调节细胞膜的离子运输,基因突变能导致蛋白产物功能的破坏或丧失。当细胞膜离子运输被中断,某些器官粘液涂层的粘度将变稠。该病的一个主要特征是呼吸道积聚厚厚的粘液,导致呼吸困难及反复感染。
 扫一扫
扫一扫