希望在临床
参加临床试验不是做小白鼠,恰恰相反,最好的,最昂贵的,最先进的,最有希望的治疗方法,都在临床试验中!
受益于中国的经济发展,很多全球性的制药巨头,为了加速新药在中国市场的上市进度,把中国纳入到全球多中心新药临床试验范围,很多新药在中国和欧美发达国家同步进行上市前的临床医学研究,以获得上市注册数据,加快上市申报进程。另外受益于中国本土制药企业的发展,以及国家对国产替代和中国创新的扶持,中国本土药企的新药临床试验也在增长。这给了患者新的希望和机会。对于因为无药可治,和无法负担治疗费用的患者家庭,参加新药临床试验:
- 既可以免费得到最新最先进的医学治疗
- 也可以免费得到中国最顶级医疗专家组的诊治
- 同时帮助低收入家庭节省数以十万计的治疗费用
查询→新药临床试验 | 争取→更多治疗机会
- 招募患者|GABAA治疗抑郁症临床试验
- 招募患者|Baxdrostat治疗高血压伴慢阻肺临床研究

- 招募患者|抗ATTR单抗治疗特应性皮炎临床试验

- 招募患者|CCR2阻滞剂治疗局灶性节段性肾小球硬化症(FSGS)临床试验

- 招募患者|ATTR消耗剂治疗经确诊的野生型或遗传型转甲状腺素蛋白(TTR)介导的淀粉样变性(ATTR)临床试验

- 招募患者|地舒单抗治疗骨巨细胞瘤临床研究

- 招募患者|ADCC单抗治疗晚期不可切除的胃或胃食管交界部腺癌临床试验

- 招募患者|KRAS抑制剂治疗KRAS-G12C突变的软组织肉瘤临床研究

- 招募患者|贝派度酸治疗高脂血症临床研究
- 招募患者|曲普瑞林治疗儿童中枢性性早熟临床研究

- 招募患者|口服PCSK9小分子抑制剂治疗经治低密度脂蛋白胆固醇未达标的血脂异常临床研究

- 招募患者|JAK1/JAK2抑制剂治疗12岁及以上成人和儿童患者的非节段性白癜风临床研究

- 招募患者|抗Nectin-4治疗晚期经治尿路上皮癌临床研究

- 招募患者|妥拉美替尼治疗BRAFV600E突变转移性结直肠癌临床试验

- 招募患者|抗Nectin-4治疗晚期实体瘤临床研究

- 招募患者|QLS1103片治疗晚期实体瘤临床研究

- 招募患者|三价伊立替康治疗小细胞肺癌临床试验

- 招募患者|溶瘤腺病毒治疗晚期实体瘤临床试验

- 招募患者|IL-4/IL-13/TSLP三抗治疗中度至重度特应性皮炎临床试验

- 招募患者|核酸内切酶抑制剂治疗存在流感并发症高风险的成人和12岁及以上青少年流感患者临床研究

- 招募患者|抗抑郁药治疗产后抑郁临床研究

- 招募患者|生长素治疗内源性生长激素缺乏所造成的儿童生长障碍临床研究
- 招募患者|瑞卢戈利治疗子宫肌瘤相关的大量月经出血临床研究

- 招募患者|长效FSH-CTP治疗特发性低促性腺激素性性腺功能减退症(IHH)临床试验

- 招募学员|10月25日开课:人工智能+影像组学&病理组学应用培训班

- 招募患者|抗OX40单抗治疗中重度特应性皮炎临床研究

- 招募患者|恩那度司他治疗非髓系恶性肿瘤患者化疗引起的贫血临床研究
- 招募患者|本维莫德喷雾剂治疗成人头皮脂溢性皮炎临床研究

- 招募患者|ADC单抗治疗复发或转移性宫颈癌临床试验

- 招募患者|NGF抑制剂治疗骨转移癌痛临床研究

- 招募患者|羟甲唑啉滴眼液治疗获得性上睑下垂临床试验

- 招募患者|白介素4治疗6-18岁中重度特应性皮炎临床试验

- 招募患者|非奈利酮治疗1型糖尿病合并慢性肾病临床试验
- 招募患者|Sacituzumab Tirumotecan治疗PD-L1 TPS≥50%转移性非小细胞肺癌临床试验

- 招募患者|Sacituzumab Tirumotecan治疗经治EGFR转移性非小细胞肺癌临床试验
- 招募患者|布立西坦辅助治疗2岁及以上部分性发作的癫痫临床试验
- 招募患者|白介素17治疗强直性脊柱炎临床试验

- 招募患者|RP901治疗膝骨关节炎(OA)临床试验

- 招募患者|布地格福吸入气雾剂治疗慢性阻塞性肺临床试验

- 招募患者|CGRP拮抗剂治疗偏头痛急性发作临床试验

- 招募患者|Risankizumab治疗中度至重度活动性克罗恩病癌临床试验
- 结束|Lepodisiran治疗动脉粥样硬化性心血管疾病(ASCVD)MACE风险临床试验

- 招募患者|奥希替尼放化疗前诱导治疗和维持治疗EGFR阳性III期不可切除非小细胞肺癌临床试验

- 招募患者|EGFR抑制剂治疗初治EGFR20突变非小细胞肺癌临床试验

- 招募患者|艾帕洛利单抗/托沃瑞利单抗治疗无EGFR敏感突变和ALK融合非小细胞肺癌临床试验

- 招募患者|奥马环素治疗成人社区获得性细菌性肺炎(CABP)临床试验

- 招募患者|多靶点TKI治疗FGFR1-3突变的经治胰腺癌临床试验

- 招募患者|P2X3受体拮抗剂治疗难治性或不明原因慢性咳嗽临床试验

- 招募患者|LFA-1拮抗剂治疗干眼症(DED)临床试验

- 招募患者|Litifilimab治疗正在接受非生物制剂标准疗法的成人活动期系统性红斑狼疮(SLE)临床试验

- 招募患者|乌帕替尼治疗系统性红斑狼疮临床试验
- 招募患者|Amlitelimab治疗18岁及以上中重度特应性皮炎临床试验

- 招募患者|Ensifentrine治疗慢性阻塞性肺病临床试验

- 招募患者|Tulisokibart治疗中度至重度溃疡性结肠炎临床试验

- 招募患者|TYK2抑制剂治疗中重度斑块状银屑病临床试验

- 招募患者|Amlitelimab治疗18岁及以上特应性皮炎临床试验

- 招募患者|Litifilimab治疗活动性亚急性皮肤型红斑狼疮(SCLE)和或慢性皮肤型红斑狼疮(CCLE)临床试验

- 招募患者|免疫调节剂治疗非感染性前葡萄膜炎临床试验

- 招募患者|基因疗法治疗年龄相关黄斑变性(AMD)中地图样萎缩(GA)临床试验

- 招募患者|布地奈德/沙丁胺醇用于18岁以上哮喘患者按需治疗或预防支气管收缩以及降低急性发作风险临床试验

- 招募患者|阿柏西普治疗糖尿病性黄斑水肿临床试验
- 招募患者|Vixarelimab治疗溃疡性结肠炎(UC)临床试验

- 招募患者|Frexalimab治疗复发型多发性硬化临床试验

- 招募患者|Tinlarebant治疗年龄相关黄斑变性(AMD)中地图样萎缩(GA)临床试验

- 终止|Sisunatovir治疗呼吸道合胞病毒(RSV)临床试验

- 招募患者|奥马珠单抗治疗慢性自发性荨麻疹临床试验
- 招募患者|P2X3拮抗剂治疗难治性慢性咳嗽临床试验

- 招募患者|白介素-2治疗系统性红斑狼疮临床试验

- 招募患者|基因疗法治疗湿性年龄相关性黄斑变性(wAMD)临床试验

- 招募患者|lgE单抗治疗过敏性哮喘临床试验

- 招募患者|TYK2抑制剂治疗银屑病关节炎临床试验

- 招募患者|伏环孢素治疗活动性狼疮肾炎临床试验

- 招募患者|毛果芸香碱滴眼液治疗成人老视(老花眼)临床试验

- 招募患者|基因疗法治疗I型戈谢病临床试验

- 招募患者|CD20单抗治疗视神经脊髓炎谱系疾病临床试验

- 招募患者|双鱼颗粒治疗流行性感冒(风热犯卫证)临床试验

- 招募患者|HSA-rhGH治疗因内源性生长激素缺乏所造成的儿童生长障碍临床试验

- 招募患者|司库奇尤单抗治疗中重度斑块状银屑病临床试验

- 结束|Orforglipron治疗肥胖或超重临床试验

- 招募患者|Giredestrant治疗ER阳性/HER2阴性晚期乳腺癌临床试验

- 招募患者|PHESGO治疗携带PIK3CA突变的HER2阳性局部晚期或转移性乳腺癌临床试验

- 招募患者|LAG-3单抗治疗微卫星稳定型/错配修复完整型结肠直肠癌临床试验
- 招募患者|苏金单抗生物类似药治疗中度至重度斑块状银屑病临床试验

- 招募患者|JAK/TYK2抑制剂治疗非节段型白癜风临床试验

- 招募患者|A型肉毒毒素治疗三叉神经痛临床试验

- 招募患者|Tarlatamab治疗局限期小细胞肺癌(LS-SCLC)临床试验

- 招募患者|索托拉西布治疗PD-L1阴性且KRAS_p.G12C阳性的非小细胞肺癌临床试验

- 招募患者|溶栓药治疗急性缺血性脑卒中临床试验

- 结束|Comekibart治疗特应性皮炎临床试验

- 招募患者|9价疫苗预防侵袭性肠外致病性大肠埃希菌疾病(IED)临床试验
- 招募患者|帕博利珠单抗/放化疗/奥拉帕利治疗未经治疗局限期小细胞肺癌(LS-SCLC)临床试验
- 结束|Tarlatamab治疗广泛期小细胞肺癌临床试验

- 结束|阿替利珠单抗治疗晚期PD-L1阳性非鳞非小细胞肺癌临床试验

- 招募患者|TROP2-ADC治疗EGFR突变非鳞状非小细胞肺癌临床试验

- 招募患者|Talquetamab治疗复发/难治性多发性骨髓瘤临床试验
- 招募患者|Nipocalimab治疗温抗体型自身免疫性溶血性贫血临床试验

- 招募患者|LUSPATERCEPT治疗JAK2抑制剂治疗中且需要输注红细胞(RBC)的骨髓增殖性肿瘤(MPN)相关骨髓纤维化(MF)临床试验

- 结束|Favezelimab治疗经典型霍奇金淋巴瘤临床试验

- 招募患者|CLL1/CD3双抗治疗急性髓性白血病/骨髓增生异常综合征1期临床试验

- 招募患者|CAR-T-19治疗25岁(含)以下CD19阳性复发/难治B细胞急性淋巴细胞白血病Ⅱ期临床试验

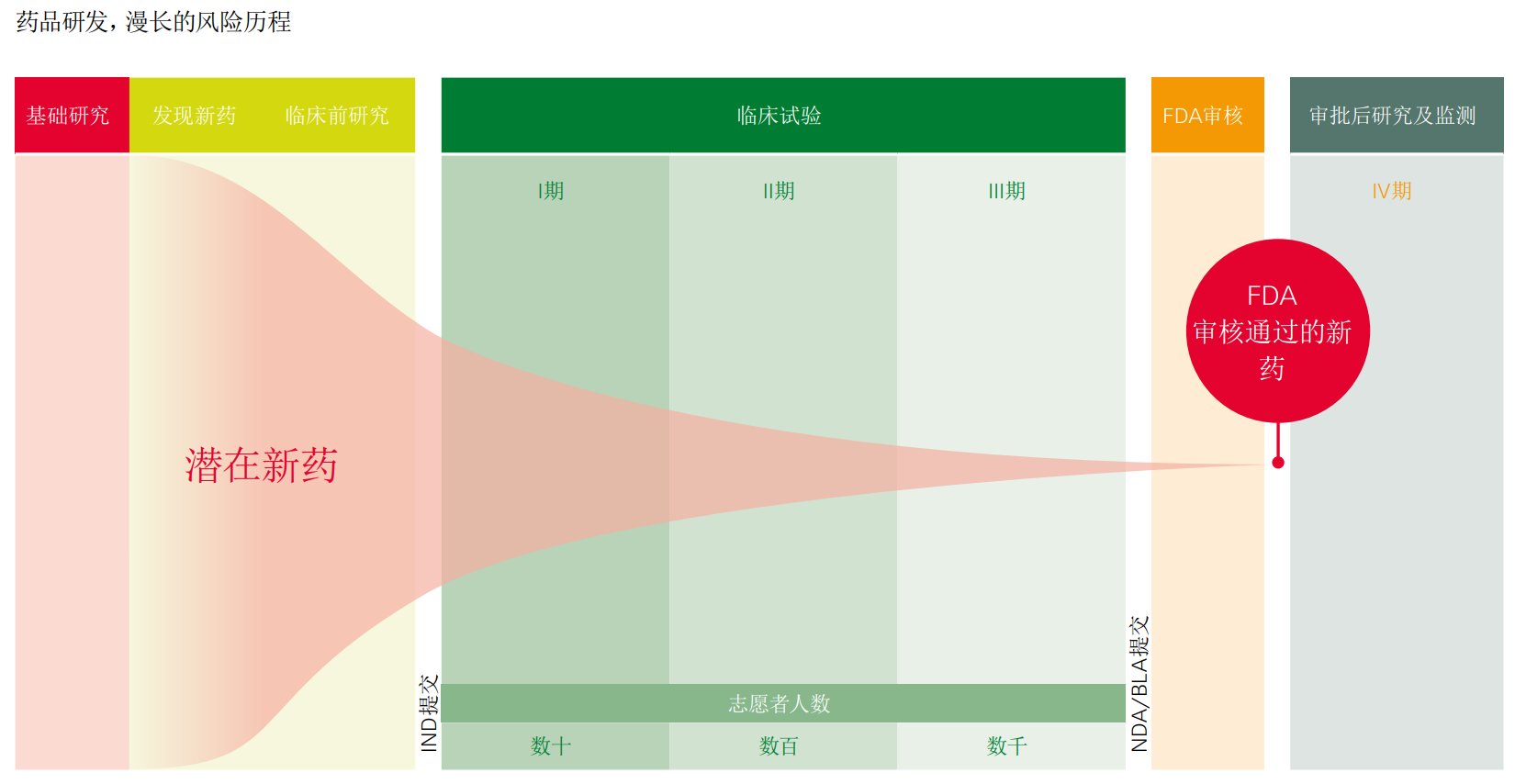
什么是新药临床试验?
药物临床试验是为了研究新药有效性和安全性。
进行药物临床试验需要多种专业技术人员组建临床研究团队,包括医学、药学、药理学、生物学、生物统计学等专业人员。
由于新药临床研究的方法、手段、目的的特殊性,需要人类受试者的参与、药物临床试验的资料和结果都需要经过药品监督管理部门的审批,遵循三项基本原则:
- 伦理道德原则
- 科学性原则
- GCP与现行法律法规
【1期】I期临床试验
初步的临床药理学及人体安全性评价试验,为新药人体试验的起始期,又称为早期人体试验。
- I期临床试验包括耐受性试验和药代动力学研究,一般在健康受试者中进行。其目的是研究人体对药物的耐受程度,并通过药物代谢动力学研究,了解药物在人体内的吸收、分布、消除的规律,为制定给药方案提供依据,以便进一步进行治疗试验。
- I 期临床试验一般从单剂量开始,在严格控制的条件下,给少量试验药物于少数(10〜100例)经过谨慎选择和筛选出的健康志愿者(对肿瘤药物而言通常为肿瘤病人),然后仔细监测药物的血液浓度、排泄性质和任何有益反应或不良作用,以评价药物在人体内的药代动力学和耐受性。通常要求志愿者在研究期间住院,每天对其进行24h的密切监护。随着对新药的安全性了解的增加,给药的剂量可逐渐提高,并可以多剂量给药。
【2期】II期临床试验
II期临床试验为治疗作用初步评价阶段。
- 其目的是初步评价药物对目标适应症患者的治疗作用和安全性,也包括为III期临床试验研究设计和给药剂量方案的确定提供依据。此阶段的研究设计可以根据具体的研究目的,采用多种形式,包括随机盲法对照临床试验。
本期临床研究重点在于药物的安全性和疗效。
- 应用安慰剂或已上市药物作为对照药物对新药的疗效进行评价,在此过程中对疾病的发生发展过程对药物疗效的影响进行研究;确定III期临床试验的给药剂量和方案;获得更多的药物安全性方面的资料。
【3期】III期临床试验
治疗作用确证阶段。其目的是进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据。
III期临床试验的目标是:
- 增加患者接触试验药物的机会,既要增加受试者的人数,还要增加受试者用药的时间;
- 对不同的患者人群确定理想的用药剂量方案;
- 评价试验药物在治疗目标适应症时的总体疗效和安全性。
该阶段是临床研究项目的最繁忙和任务最集中的部分。
【4期】IV期临床试验
上市后的研究在国际上多数国家称为“ IV期临床试验”。
新药在获准上市后,仍然需要进行进一步的研究,在广泛使用条件下考察其疗效和不良反应。
在上市前进行的前三期临床试验是对较小范围、特殊群体的病人进行的药品评价,病人是经过严格选择和控制的,因此有很多例外。
而上市后,许多不同类型的病人将接受该药品的治疗。所以很有必要重新评价药品对大多数病人的疗效和耐受性。在上市后的IV期临床研究中,数以千计的经该药品治疗的病人的研究数据被收集并进行分析。在上市前的临床研究中因发生率太低而没有被发现的不良反应就可能被发现。这些数据将支持临床试验中巳得到的数据,可以使药厂让医生能够更好地和更可靠地认识到该药品对“普通人群” 的治疗受益-风险比。
新适应症研究
进行上市后研究的另一目的是进一步拓宽药品的适应症范围。在产品许可证中清楚地限定了药品的适应症,该药品也可能用于除此之外的其他适应症,但必须首先有临床试验的数据。
- 在有的国家将这种新适应症的临床研究也归为“ IV期临床试验”
- 但也有国家将其称为“III期临床试验B” (Phase IIIB)
- 那么相应的第一适应症的III期临床试验就被称为“ III期临床试验A” (Phase IIIA)
 扫一扫
扫一扫 




