2023年08月14日(纽约)专注于治疗原发性和转移性肝癌的介入肿瘤公司Delcath Systems公司宣布,美国FDA已批准Hepzato系统(melphalan/肝脏输送系统)作为转移性葡萄膜恶性黑色素瘤(mUM)成人患者的肝导向治疗。这些患者不可切除的肝转移病变影响肝脏不足50%,且没有肝外疾病,或肝外疾病仅限于骨骼、淋巴结、皮下组织或肺部,且适于切除或放射治疗。
- Hepzato系统是FDA批准用于mUM治疗的首款肝导向疗法。
FDA的批准主要基于FOCUS研究的结果,这是一项单臂、多中心、开放标签3期临床研究。91名患者每6至8周接受治疗,最多接受6次治疗。主要的疗效终点是由独立审查委员会评估的客观缓解率(ORR)和缓解持续时间(DoR)。试验结果显示,ORR为36.3%(95% CI:26.4,47.0),包含7例完全缓解,中位DoR为14个月(95% CI:8.3,17.7)。在接受治疗的患者中观察到的疾病控制率(DCR)为73.6%(95% CI:63.3,82.3)。
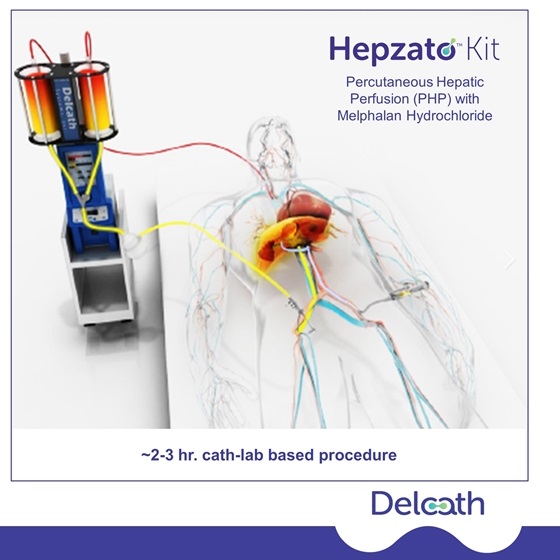
HEPZATO KIT 系统是一个组合产品,通过Delcath的肝脏输送系统直接将已经获批的化疗药物美法仑(melphalan)输送到肝脏。该系统允许更高的目标药物暴露组织,同时限制全身毒性。HDS 的使用使医疗保健提供者团队能够通过手术隔离肝脏,同时在马法兰输注期间过滤肝静脉血,并在经皮肝灌注 (PHP) 手术期间进行随后的冲洗。PHP 只能使用 Delcath 的 HDS 进行,导致局部区域输送相对较高的美法仑剂量。
肝为主的转移性葡萄膜黑色素瘤(Hepatic-Dominant Metastatic Uveal Melanoma)mUM是一种罕见且具有侵袭性的转移性癌症,在美国每年发病率约为 1,000 例。百分之九十的 mUM 涉及肝脏,而肝功能衰竭往往是死亡原因。美国国家综合癌症网络 (NCCN) 指南建议对患有肝转移的 mUM 患者进行肝脏定向治疗。HEPZATO KIT 是 FDA 批准的唯一1种用于治疗 mUM 的肝脏定向疗法,而 HEPZATO KIT 实现的经皮肝灌注 (PHP) 程序已纳入 NCCN 指南。
| 信息 | 来源 |
| Delcath Systems, Inc. Announces FDA Approval of HEPZATO KIT™ for the Treatment of Adult Patients with Unresectable Hepatic-Dominant Metastatic Uveal Melanoma | https://www.prnewswire.com/news-releases/delcath-systems-inc-announces-fda-approval-of-hepzato-kit-for-the-treatment-of-adult-patients-with-unresectable-hepatic-dominant-metastatic-uveal-melanoma-301900346.html |
| 免责声明 | 本资料仅作参考,诊疗请遵医嘱。 |
 扫一扫
扫一扫 


